Il pancreas artificiale: da sogno a realtà
La lunga strada nello sviluppo di un sistema automatico per la gestione della glicemia.
Il diabete mellito di tipo 1 è una malattia cronica associata ad un aumento di morbidità e mortalità e a una ridotta qualità della vita. Il buon controllo glicemico riduce le complicanze associate al diabete ma al prezzo di un aumentato rischio di ipoglicemia
Nonostante i progressi nelle formulazioni insuliniche e nella tecnologia (microinfusori intelligenti, dispositivi per il monitoraggio continuo della glicemia, sistemi integrati microinfusore + sensore), il target glicemico resta difficile da raggiungere e molti pazienti trascorrono diverse ore della giornata in ipo o iperglicemia.
Da qui l’idea di sostituire la funzione beta cellulare deficitaria con il pancreas artificiale (PA), cioè con un sistema automatico in grado di regolare la somministrazione di insulina sulla base dei valori glicemici rilevati in tempo reale dal sensore, sotto la supervisione di un algoritmo matematico che funge da controllore esterno
Rispetto ai primi modelli di pancreas artificiale, risalenti agli anni 80, ingombranti e di uso puramente sperimentale, lo sviluppo tecnologico dell’ultimo decennio ha permesso di realizzare un modello di pancreas artificiale utilizzabile dal paziente nella vita di tutti i giorni. Esso è costituito da un microinfusore per la somministrazione sottocutanea continua di insulina, un sensore per il monitoraggio continuo della glicemia a livello sottocutaneo (CGM) e un algoritmo di controllo, che rappresenta “il cervello” del pancreas artificiale.
Sono stati sviluppati vari modelli di algoritmo ma il più utilizzato è il Model Predictive Control (MPC), o algoritmo di controllo predittivo, che regola l’infusione di insulina sulla base della glicemia (precedente, attuale e prevista) e di parametri individuali del paziente (rapporto insulina/carboidrati, fattore di correzione…), ed è costruito su princìpi basati sulla fisiopatologia del diabete, sull’analisi di fattori confondenti e sull’identificazione di eventuali errori.
Nei primi prototipi di pancreas artificiale, l’algoritmo di controllo era installato in un computer portatile collegato via cavo al dispositivo per CGM e al microinfusore. Con questo sistema, sono stati condotti diversi studi preliminari, in ambito ospedaliero, al fine di testarne sicurezza ed efficacia. Gli studi hanno dimostrato la superiorità del PA, rispetto alla terapia con microinfusore, nel controllare la glicemia e nel ridurre le ipoglicemie. Il sistema utilizzato era, peraltro, troppo ingombrante per essere utilizzato nella vita di tutti i giorni. Un passo avanti è stato compiuto inserendo l’algoritmo in un telefono cellulare, privato delle funzioni classiche di telefono, in grado di comunicare via bluetooth con gli altri componenti del PA (Figura 1).
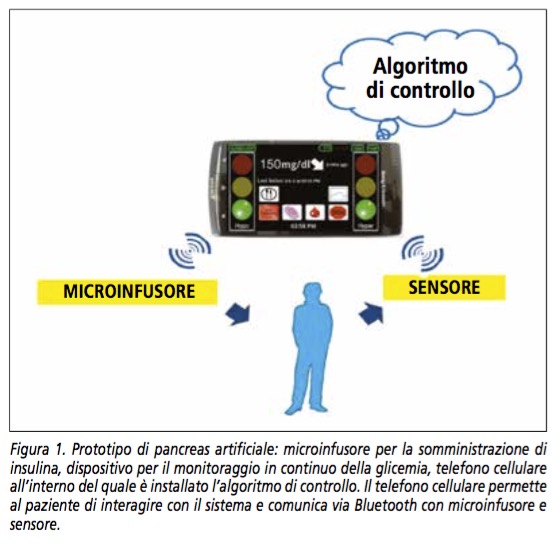
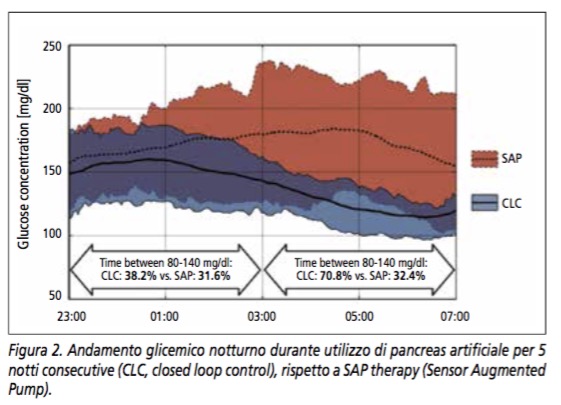
Con questo sistema sono stati intrapresi i primi studi in ambito extra ospedaliero seppure, inizialmente, in ambiente protetto, come ad esempio in un hotel o durante campi scuola, dove, oltre al paziente, risiedevano anche medici e ingegneri, pronti a intervenire per qualsiasi necessità. Questi studi hanno confermato l’efficacia terapeutica del sistema e ne hanno dimostrato la fattibilità e semplicità di utilizzo da parte del paziente. Il nostro gruppo di studio, ad esempio, che collabora con le Scuole di Ingegneria delle Università di Padova (Prof. Claudio Cobelli) e Pavia (Prof. Lalo Magni) e con i colleghi dell’Università della Virginia, ha confrontato l’utilizzo del PA per 5 notti consecutive trascorse in hotel rispetto a 5 notti di terapia con microinfusore e sensore (Figura 2), dimostrando che con il PA si otteneva un aumento del tempo nel range glicemico compreso tra 80-140mg/dl (54.5% vs. 32.2%, p<0.001), una riduzione della glicemia media durante la notte (139.0 vs. 170.3mg/dl, p<0.001) ed un miglioramento della glicemia al risveglio (119.3 vs. 152.9mg/dl, p<0.001).
Altri gruppi hanno testato il sistema in adolescenti durante un campo scuola ottenendo gli stessi risultati, pur utilizzando un algoritmo diverso dal “MPC”, di tipo “fuzzy logic”, che mira ad emulare in modo automatico il ragionamento di un esperto diabetologo
Questi soddisfacenti risultati hanno incoraggiato i ricercatori a testare il sistema in condizioni di free living, a casa del paziente. A tal fine, il gruppo inglese, diretto dal Prof. Roman Hovorka, ha sottoposto 24 adulti e 16 adolescenti a due periodi di studio in cui, a domicilio, veniva usato microinfusore integrato a sensore (Sensor Augmented Pump, SAP therapy) combinato o no ad uso di PA durante la notte. Ciascun periodo durava 4 settimane nell’adulto e 3 settimane nell’adolescente. Gli autori hanno dimostrato che durante l’utilizzo del pancreas artificiale si osservava, rispetto a SAP therapy, una riduzione della glicemia media (142.2 vs 156.6 mg/dl, p<0.001) e un aumento del 18,4% del tempo trascorso nel range glicemico 70-140 mg/dl (59.2 vs 40.7 %, p<0.001). Il gruppo israeliano ha confermato gli stessi risultati in 24 diabetici di tipo 1 (età compresa tra i 12-43 anni) che, a domicilio, per 6 settimane, avevano utilizzato durante la notte il PA con algoritmo di tipo fuzzy logic
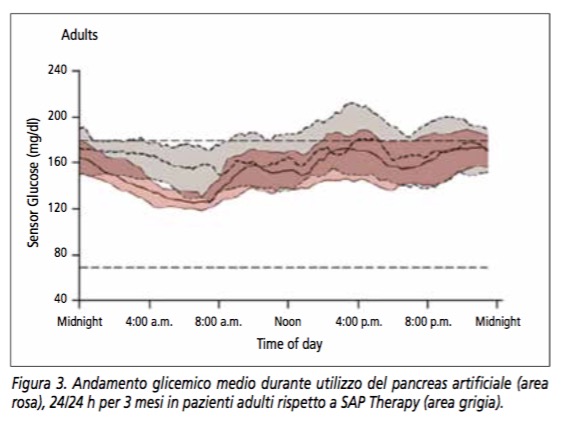
Anche il nostro gruppo, nell’ambito del progetto Europeo AP@home, ha testato l’efficacia del sistema a domicilio del paziente. Si tratta di uno studio multicentrico cui hanno partecipato anche i colleghi di Amsterdam e Montpellier. 32 pazienti con diabete di tipo 1 in terapia con microinfusore sono stati randomizzati a due diversi periodi di trattamento con microinfusore e sensore associato o meno all’utilizzo del PA dal momento della cena al mattino successivo. Il controllo del periodo postprandiale è una ulteriore sfida per il pancreas artificiale! Ciascun periodo durava 8 settimane ed era separato dal successivo da un periodo di 4 settimane di wash-out in cui il paziente proseguiva con terapia abituale. Durante l’utilizzo del pancreas artificiale, abbiamo osservato una riduzione della glicemia media (162 vs 167.4mg/dl, p=0.0053), un aumento del tempo trascorso nel target 80-140 mg/dl (37.7 vs 31.2% p<0.0001), una riduzione del tempo trascorso in iperglicemia >180 (31.6 vs 38.5%, p<0.0001) e in ipoglicemia <70 mg/dl (1.7 vs 3.0%, p<0.0001) e una riduzione dei valori di emoglobina glicata rispetto a terapia con microinfusore e sensore (riduzione HbA1c 3.5 vs 1.8 mmol/mol, p=0.047). Questi dati sono stati successivamente confermati anche durante l’utilizzo del PA giorno e notte (24/24h) per 3 mesi in 33 diabetici di tipo 1 adulti. Ancora una volta il PA permetteva, rispetto a SAP therapy, di migliorare il controllo glicemico (Figura 3) (aumento del tempo in target, riduzione della glicemia media e del tempo trascorso in ipoglicemia) riducendo, nel contempo, i valori di emoglobina glicata
Attualmente sono in corso altri studi che mirano a testare l’utilizzo del pancreas artificiale per 24/24h per periodi ancora più lunghi, al fine di verificare l’efficacia del sistema di fronte a sfide sempre più impegnative come l’attività fisica e la gestione di pasti complessi.
Al fine di ridurre ulteriormente gli episodi ipoglicemici, alcuni ricercatori hanno testato l’uso del pancreas bi-ormonale che prevede la somministrazione contemporanea di insulina e glucagone.
In un recente trial Russel et al. hanno dimostrato che l’uso per 5 giorni consecutivi del pancreas biormonale in 20 adulti e 32 adolescenti portava a un controllo glicemico e a una riduzione degli episodi ipoglicemici rispetto a quanto ottenuto durante terapia con microinfusore
Al di là degli importantissimi risultati metabolici ottenuti col pancreas uni o bi ormonale, è altrettanto rilevante l’aspetto umano, il vissuto dei pazienti che, dall’uso del pancreas artificiale, riportano un grande senso di libertà, sicurezza e tranquillità.
Il pancreas artificiale, quindi, non è più da considerare un sogno ma una prossima realtà, in grado di migliorare i profili glicemici e la qualità della vita dei nostri pazienti.
Federico Boscari
Silvia Galasso
Angelo Avogar
Daniela Bruttomesso
Dipartimento di Medicina Clinica
UOC Diabetologia e Malattie del Metabolismo
Università di Padova
Tratto da: Cardiolink, 20 luglio 2016

